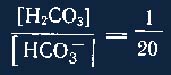
2.2. Механизмы поддержания кислотно-основного состояния организма
Основные механизмы элиминации кислых продуктов жизнедеятельности следующие: буферирование, экскреция СО2 легкими и экскреция фиксированных кислот почками.
Буферные системы. Главным буфером плазмы и интерстициальной жидкости является бикарбонат (НСО3—). В клетках тканей, эритроцитах преобладают белковая буферная система (включая гемоглобин, частично определяющий буферные свойства внеклеточной жидкости) и фосфаты. Фактором, определяющим равновесие между буферными системами, является рН. В качестве материала для изучения и оценки активности буферных систем организма в клинической практике исследуется кровь. В известной мере это ограничивает возможность суждения о буферных свойствах белков и фосфатов, но вместе с тем обеспечивает возможность оценки главного буфера — бикарбоната и, следовательно, оценки всего кислотно-основного баланса.
Для простоты буферные системы крови могут быть разделены на две группы: бикарбонатную и небикарбонатную (гемоглобин) буферные системы. В соответствии с этим буферирование и транспорт угольной кислоты (в виде НСО3—) может происходить при участии небикарбонатных буферных систем по следующей схеме:
Н2СО3 + Буфер— →Буфер + НСО3—
СО2 поступает из тканей в легкие главным образом в форме бикарбоната плазмы, образовавшегося внутри эритроцита в процессе буферирования угольной кислоты гемоглобином. Оставшаяся часть существует в крови в виде карбаминовых соединений и растворенной СО2. Эти реакции в легочных капиллярах происходят в обратном порядке, и СО2 экскретируется легкими со скоростью, определяемой темпом ее образования в организме.
Буферирование фиксированных кислот происходит с участием бикарбонатного буфера в форме образования угольной кислоты:
Н+ + НСО3— →Н2СО3
или с участием небикарбонатного буфера:
Н+•Буфер— → Н • Буфер
Буферные основания Буферные кислоты
Продукция эндогенных Н+ (т. е. фиксированных кислот) может буферироваться как бикарбонатной, так и небикарбонатной буферными системами, в результате чего буферные основания превращаются в буферные кислоты. Восполнение теряемых при этом буферных оснований прямо зависит от способности дистальных почечных канальцев синтезировать бикарбонат. Это непременное условие выделения Н+ почками.
В процессах буферирования фиксированных кислот бикарбонатная система количественно является наиболее важной.
В каждой цельной буферной системе (т. е. смеси слабой кислоты и ее соли с сильным основанием) соотношение между кислотным и основным компонентами не равнозначно. Так, в бикарбонатной системе:
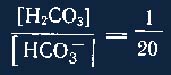
Именно этим отношением (т. е. явным преобладанием основного компонента над кислотным) и определяется величина рН, равная в норме 7,4. Как известно, концентрация свободных водородных ионов в бикарбонатной буферной системе может быть вычислена по формуле:
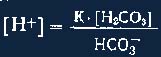
где К — константа диссоциации.
После логарифмирования это уравнение может быть записано так:
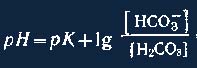
где рН= — lg [H+]; рК=— IgK. Это уравнение называется уравнением Гендерсона — Гассельбалха.
[Н2СО3] может быть заменен выражением Рсо2-0,03, так как Н2СО3 находится в равновесии с растворенной СО2, которая в свою очередь .находится в равновесии с альвеолярным или тканевым Рсо2. В представленном выражении 0,03 [ммоль/(л-мм рт. ст.)] является коэффициентом растворимости СО2 в плазме при 37 °С.
Следовательно:
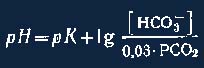
Так как в нормальных условиях рК составляет 6,1, а [НСО3~] 25 ммоль/л и РСО2 40 мм рт. ст., то:
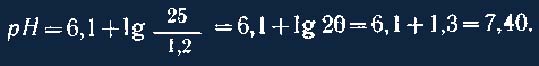
Отсюда ясно,
что при увеличении содержания угольной кислоты в организме отношение
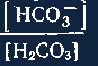 станет
меньше, чем 20:1, логарифм этого отношения станет меньше 1,3 и рН снизится, что
будет отражать степень возникшего ацидоза. Наоборот, при увеличении содержания
основной соли (бикарбонат) в крови отношение
станет
меньше, чем 20:1, логарифм этого отношения станет меньше 1,3 и рН снизится, что
будет отражать степень возникшего ацидоза. Наоборот, при увеличении содержания
основной соли (бикарбонат) в крови отношение 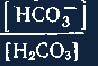 станет
большим, чем 20: 1, логарифм отношения
i-----L-l_
увеличится до 1,4—1,5, рН возрастет до 7,5—7,6, что будет характеризовать
степень возникшего алкалоза.
станет
большим, чем 20: 1, логарифм отношения
i-----L-l_
увеличится до 1,4—1,5, рН возрастет до 7,5—7,6, что будет характеризовать
степень возникшего алкалоза.
Эта
же формула позволяет понять, что снижение рН возможно не только при увеличении
содержания Н2СО3, но и при уменьшении содержания НСОз
отношение (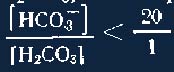 ),
а возрастание рН возможно
не только при увеличении содержания в крови бикарбоната, но и при уменьшении
содержания угольной кислоты (отношение
),
а возрастание рН возможно
не только при увеличении содержания в крови бикарбоната, но и при уменьшении
содержания угольной кислоты (отношение
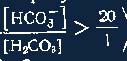
Дыхательная регуляция КОС. Основная роль легких в отношении кислотно-основного гомеостаза состоит в экскреции СО2 и стабилизации РСО2 артериальной крови (Расо,) около . 40 мм рт. ст. При нормальной функции легких альвеолярное Рсо2 и Рас0; фактически идентичны. Экскреция СО2 равна продукции СО2. Следовательно:
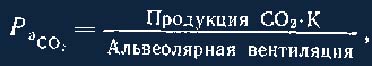
где К — коэффициент пропорциональности.
Дыхательный центр быстро реагирует на малейшие изменения РаСО2, поэтому всякие изменения продукции СО2 в организме сопровождаются соответствующими изменениями альвеолярной вентиляции.
Почечная регуляция КОС. Почки участвуют в регуляции КОС путем стабилизации содержания [НСО3—] плазмы на уровне, близком к 22—26 ммоль/л. Основной механизм почечной регуляции связан с выведением Н+ через клетки почечных канальцев, образующихся из угольной кислоты, а также с задержкой Na+ в канальцевой жидкости (моча). Конечный результат зависит от характера буфера в канальцевой моче. Каждый миллимоль Н+, экскретируемых в форме титруемых iкислот и (или) ионов аммония (NH4+) добавляет в плазму крови 1 ммоль НСО3—. Таким образом, экскреция Н+ теснейшим образом связана с синтезом НСО3—. Количество синтезируемого бикарбоната обычно достаточно, чтобы пополнить израсходованное на нейтрализацию титруемых кислот и на буферирование эндогенного Н+. При расстройствах КОС почки могут регулировать экскрецию Н+, чтобы поддержать необходимую концентрацию его во внеклеточной жидкости или чтобы восстановить нарушенный его баланс.
Почечная регуляция КОС является медленным процессом, требующим часов и даже дней для полной компенсации, и лишь финальным этапом элиминации кислот из организма.
Существуют четыре возможных варианта расстройств кислотно-основного состояния: респираторные ацидоз и алкалоз, метаболические ацидоз и алкалоз (табл. 2.2).
Респираторные расстройства КОС начинаются с изменений Рсо2. Для компенсации включаются буферные или почечные механизмы, которые приводят к изменениям концентрации НСО3—, способствующим восстановлению рН до исходных (хотя не всегда нормальных) величин.
Метаболические расстройства вызываются изменениями содержания в плазме НСО3—. Они индуцируют дыхательный ответ, который приводит к компенсаторному (или вторичному) изменению РСО2, в результате чего восстанавливается исходный (или нормальный) уровень рН. Таким образом, компенсаторные реакции не являются самостоятельными (или независимыми) изменениями КОС, а представляют собой непременную и ин-
тегрированную часть всего кислотно-основного баланса. Компенсаторные сдвиги КОС развиваются, как правило, немедленно и продолжаются (если сохранены резервы организма) до восстановления нормального кислотно-основного баланса, что выражается в нормализации рН.
|
● |
● |
● |
● |
● |
● |
● |
● |